2024年H1上市器械注冊(cè)半年報(bào)
發(fā)布時(shí)間:2024-08-16 瀏覽次數(shù):
2024年H1注冊(cè)備案信息匯總統(tǒng)計(jì):
-
注冊(cè)批準(zhǔn)醫(yī)療器械數(shù)量12363項(xiàng)
-
備案批準(zhǔn)醫(yī)療器械數(shù)量16941項(xiàng)
-
優(yōu)先審批注冊(cè)醫(yī)療器械產(chǎn)品58項(xiàng)
-
創(chuàng)新審批注冊(cè)醫(yī)療器械產(chǎn)品82項(xiàng)
2024年H1醫(yī)療器械注冊(cè)情況分析
據(jù)藥智醫(yī)械數(shù)據(jù)最新統(tǒng)計(jì),2024年H1全國(guó)共批準(zhǔn)注冊(cè)醫(yī)療器械12363項(xiàng),同比減少20.3%,其中優(yōu)先審批注冊(cè)58項(xiàng),創(chuàng)新審批注冊(cè)82項(xiàng);審批備案醫(yī)療器械數(shù)量16941項(xiàng),同比減少17.8%。
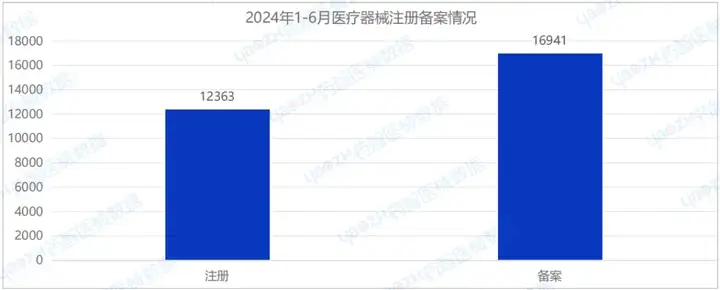
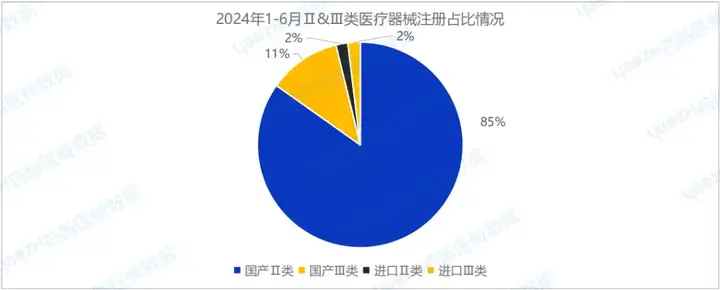
2024年H1,全國(guó)共批準(zhǔn)注冊(cè)醫(yī)療器械產(chǎn)品12363項(xiàng)。其中,國(guó)產(chǎn)第Ⅱ類(lèi)醫(yī)療器械產(chǎn)品10487項(xiàng),國(guó)產(chǎn)第Ⅲ類(lèi)醫(yī)療器械產(chǎn)品1405項(xiàng),進(jìn)口第Ⅱ類(lèi)醫(yī)療器械產(chǎn)品231項(xiàng),進(jìn)口第Ⅲ類(lèi)醫(yī)療器械產(chǎn)品240項(xiàng)。國(guó)產(chǎn)總體占比96.1%。
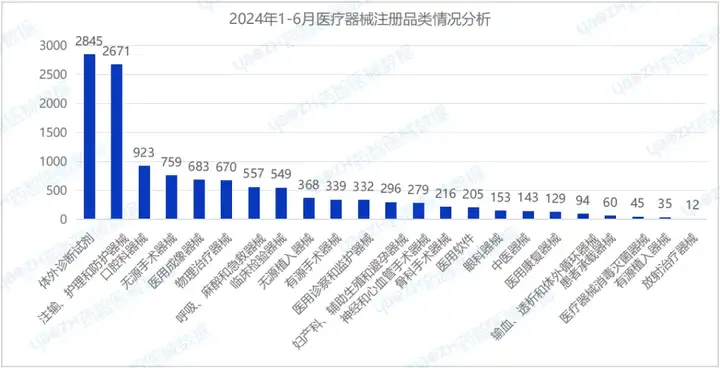
從產(chǎn)品類(lèi)別來(lái)看,2024年H1注冊(cè)醫(yī)療器械中,體外診斷試劑(2845件)、注輸、護(hù)理和防護(hù)器械(2671件)、及口腔科器械(923件)注冊(cè)數(shù)量排名前三。
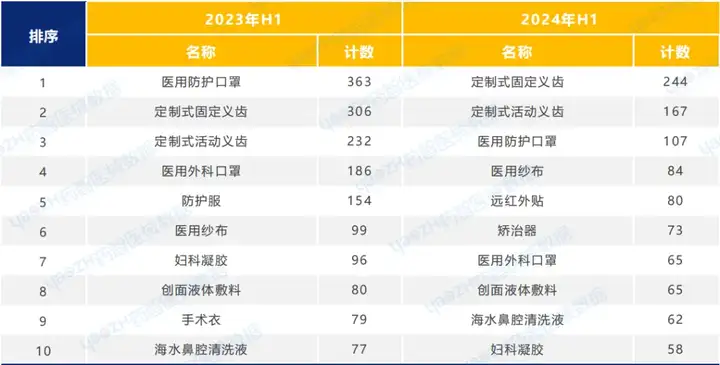
2024年H1,義齒類(lèi)口腔科醫(yī)療器械和防護(hù)類(lèi)醫(yī)療器械產(chǎn)品占醫(yī)療器械注冊(cè)產(chǎn)品數(shù)量排名靠前的位置。其中,防護(hù)類(lèi)醫(yī)療器械-醫(yī)用防護(hù)口罩較2023年同期注冊(cè)數(shù)量減少。
從國(guó)產(chǎn)Ⅱ類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品來(lái)源地分布來(lái)看,2024年H1國(guó)內(nèi)共有31個(gè)省市(不包括中國(guó)港澳臺(tái))注冊(cè)Ⅱ類(lèi)醫(yī)療器械,其中江蘇省注冊(cè)醫(yī)療器械數(shù)量最多,占國(guó)產(chǎn)Ⅱ類(lèi)醫(yī)療器械注冊(cè)數(shù)量的26.0%。

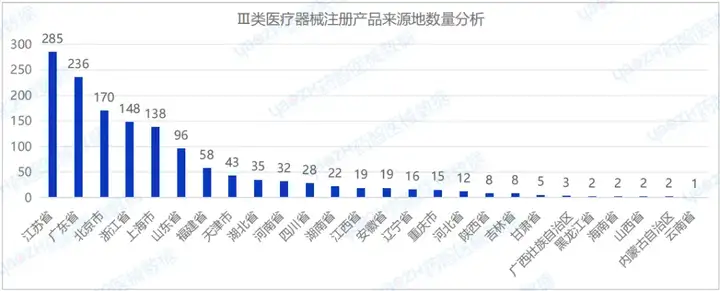
從國(guó)產(chǎn)Ⅲ類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品來(lái)源地分布來(lái)看,2024年H1國(guó)內(nèi)共有26個(gè)省市(不包括中國(guó)港澳臺(tái))注冊(cè)Ⅲ類(lèi)醫(yī)療器械,其中江蘇省注冊(cè)醫(yī)療器械數(shù)量最多,占國(guó)產(chǎn)Ⅲ類(lèi)醫(yī)療器械注冊(cè)數(shù)量的20.3%。
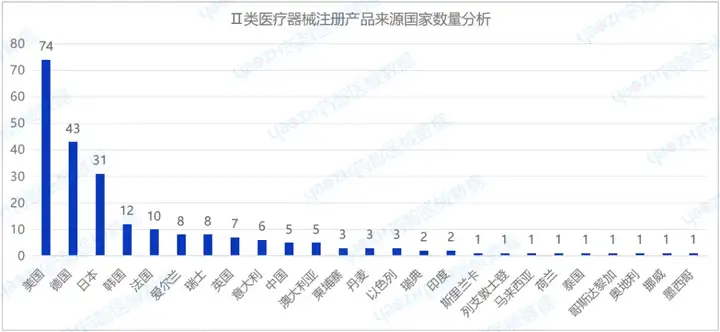
從進(jìn)口Ⅱ類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品來(lái)源國(guó)家/地區(qū)分布來(lái)看,2024年H1共有25個(gè)國(guó)家/地區(qū)(包括中國(guó)港澳臺(tái))注冊(cè)進(jìn)口Ⅱ類(lèi)醫(yī)療器械,其中美國(guó)注冊(cè)醫(yī)療器械數(shù)量最多,占進(jìn)口Ⅱ類(lèi)醫(yī)療器械注冊(cè)數(shù)量的32.0%。
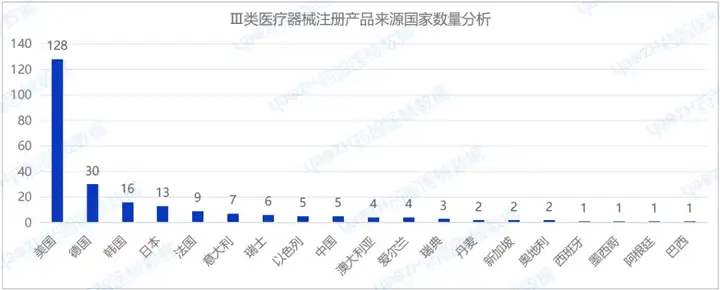
從進(jìn)口Ⅲ類(lèi)醫(yī)療器械注冊(cè)產(chǎn)品來(lái)源國(guó)家分布來(lái)看,2024年H1共有19個(gè)國(guó)家/地區(qū)(包括中國(guó)港澳臺(tái))注冊(cè)Ⅲ類(lèi)醫(yī)療器械,其中美國(guó)注冊(cè)醫(yī)療器械數(shù)量最多,占進(jìn)口Ⅲ類(lèi)醫(yī)療器械注冊(cè)數(shù)量的53.3%。
據(jù)《醫(yī)療器械監(jiān)督管理?xiàng)l例》規(guī)定,第一類(lèi)醫(yī)療器械采用產(chǎn)品備案管理方式。
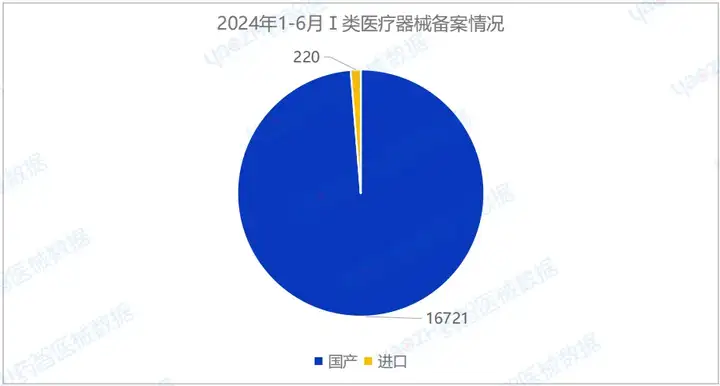
2024年H1國(guó)產(chǎn)Ⅰ類(lèi)醫(yī)療器械備案批準(zhǔn)數(shù)量16721項(xiàng),同比減少17.5%。同時(shí),進(jìn)口第一類(lèi)醫(yī)療器械備案批準(zhǔn)數(shù)量220項(xiàng),同比減少32.3%。
2024年H1醫(yī)療器械創(chuàng)新及優(yōu)先審批
根據(jù)《創(chuàng)新醫(yī)療器械特別審批程序(試行)》,我國(guó)醫(yī)療器械創(chuàng)新審批是為了保障醫(yī)療器械的安全、有效,鼓勵(lì)醫(yī)療器械的研究與創(chuàng)新,促進(jìn)醫(yī)療器械新技術(shù)的推廣和應(yīng)用,推動(dòng)醫(yī)療器械產(chǎn)業(yè)發(fā)展的特殊審批通道。
2024年H1,全國(guó)創(chuàng)新審批注冊(cè)產(chǎn)品共計(jì)82項(xiàng),包括79項(xiàng)國(guó)產(chǎn)注冊(cè)產(chǎn)品,3項(xiàng)進(jìn)口注冊(cè)產(chǎn)品。
從產(chǎn)品類(lèi)別來(lái)看:包括75項(xiàng)器械產(chǎn)品,7項(xiàng)試劑產(chǎn)品。

注:以上僅為部分產(chǎn)品信息截圖,更多創(chuàng)新審批產(chǎn)品信息請(qǐng)前往藥智醫(yī)械數(shù)據(jù)-中國(guó)器械創(chuàng)新和優(yōu)先審評(píng)數(shù)據(jù)庫(kù)查看
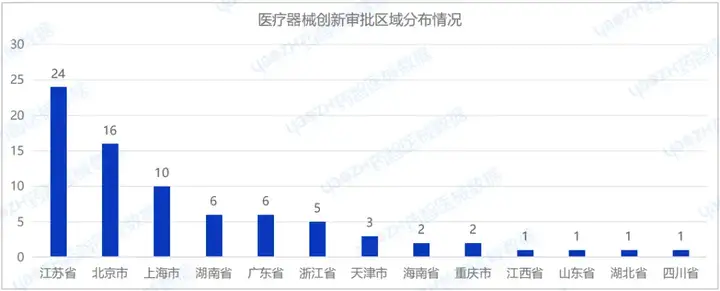
2024年H1共有13個(gè)省市注冊(cè)國(guó)產(chǎn)創(chuàng)新審批醫(yī)療器械,其中江蘇省注冊(cè)數(shù)量排名第一,為24項(xiàng)。
2016年10月25日,國(guó)家藥監(jiān)局發(fā)布《醫(yī)療器械優(yōu)先審批程序》,于2017年1月1日起施行。根據(jù)《醫(yī)療器械優(yōu)先審批程序》,對(duì)下列醫(yī)療器械實(shí)施優(yōu)先審批:
-
一是診斷或治療罕見(jiàn)病、惡性腫瘤且具有明顯臨床優(yōu)勢(shì)的醫(yī)療器械,診斷或治療老年人特有和多發(fā)疾病且尚無(wú)有效診斷或治療手段的醫(yī)療器械,專(zhuān)用于兒童且具有明顯臨床優(yōu)勢(shì)的醫(yī)療器械;
-
二是列入國(guó)家科技重大專(zhuān)項(xiàng)或國(guó)家重點(diǎn)研發(fā)計(jì)劃的醫(yī)療器械。
此外,將根據(jù)各方面情況和意見(jiàn),組織專(zhuān)家審查后,確定對(duì)“其他應(yīng)當(dāng)優(yōu)先審批的醫(yī)療器械”予以?xún)?yōu)先審批。
2024年H1,全國(guó)優(yōu)先審批注冊(cè)產(chǎn)品共計(jì)58項(xiàng),包括56項(xiàng)國(guó)產(chǎn)注冊(cè)產(chǎn)品,2項(xiàng)進(jìn)口注冊(cè)產(chǎn)品。從產(chǎn)品類(lèi)別來(lái)看:包括42項(xiàng)器械產(chǎn)品,16項(xiàng)試劑產(chǎn)品。

注:以上僅為部分產(chǎn)品信息截圖,更多優(yōu)先審批產(chǎn)品信息請(qǐng)前往藥智醫(yī)械數(shù)據(jù)-中國(guó)器械創(chuàng)新和優(yōu)先審評(píng)數(shù)據(jù)庫(kù)查看
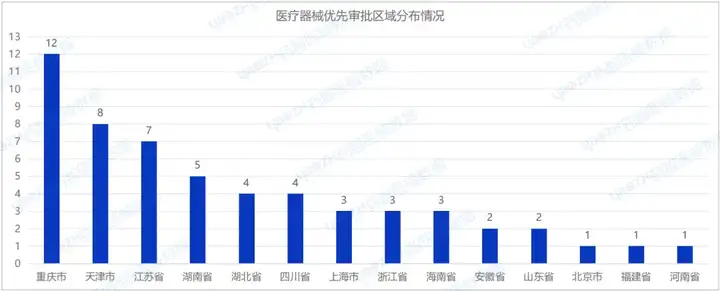
2024年H1共有14個(gè)省市注冊(cè)醫(yī)療器械進(jìn)入優(yōu)先審批,其中重慶市注冊(cè)數(shù)量排名第一,為12項(xiàng)。
2024年H1醫(yī)療器械注冊(cè)企業(yè)分析
2024年H1國(guó)內(nèi)注冊(cè)醫(yī)療器械企業(yè)達(dá)4517家。排行前十的企業(yè)中,排名前三的分別是:鄭州安圖生物工程股份有限公司、深圳市科曼醫(yī)療設(shè)備有限公司、武漢生之源生物科技股份有限公司,其中鄭州安圖生物工程股份有限公司的注冊(cè)數(shù)量排名第一,排行前十的企業(yè)情況如下圖所示。
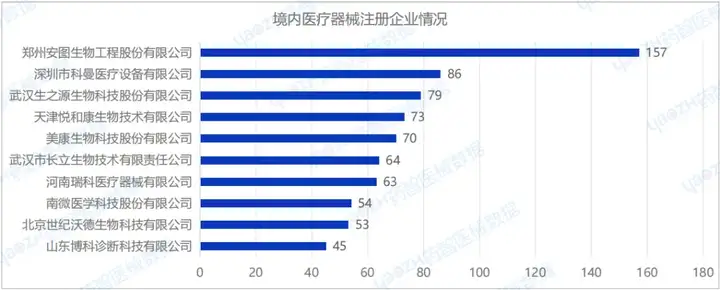
鄭州安圖生物工程股份有限公司在2024年H1共完成了157項(xiàng)醫(yī)療器械注冊(cè),注冊(cè)產(chǎn)品數(shù)量排名第一,其中包括152項(xiàng)Ⅱ類(lèi)IVD試劑產(chǎn)品,5項(xiàng)Ⅲ類(lèi)IVD試劑產(chǎn)品。
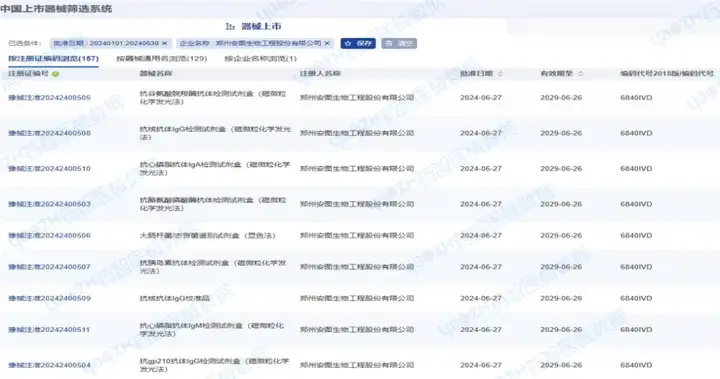
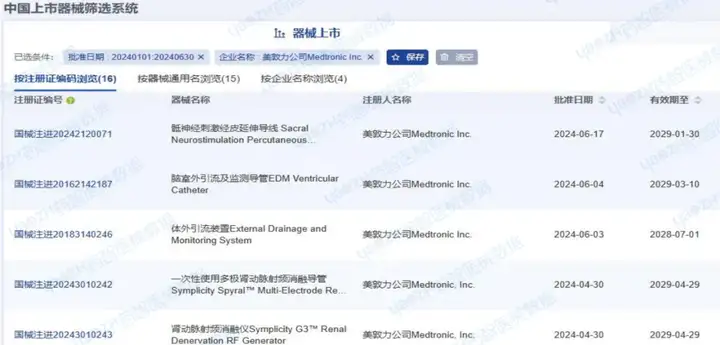
注:以上僅為部分產(chǎn)品信息截圖,更多企業(yè)產(chǎn)品注冊(cè)信息請(qǐng)前往藥智醫(yī)械數(shù)據(jù)-中國(guó)上市器械篩選系統(tǒng)查看
2024年H1國(guó)內(nèi)注冊(cè)進(jìn)口醫(yī)療器械企業(yè)達(dá)272家。排行前十的企業(yè)中,排名前三的分別是:美敦力公司(Medtronic Inc.)、歐根泰克診斷股份有限公司(ORGENTEC Diagnostika GmbH)、波士頓科學(xué)公司(Boston Scientific Corporation),其中美敦力公司(Medtronic Inc.)注冊(cè)產(chǎn)品數(shù)量排名第一,排行前十的企業(yè)情況如下圖所示。
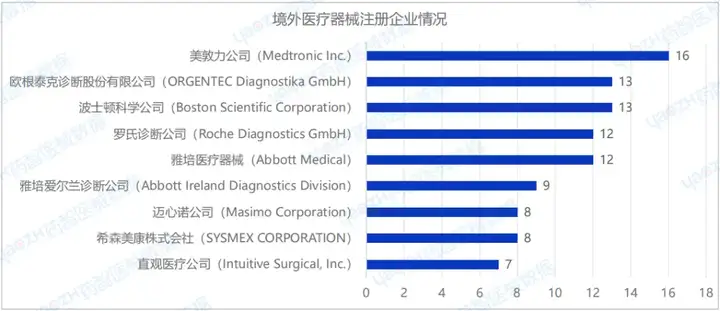
2024年H1,美敦力公司(Medtronic Inc.)注冊(cè)16項(xiàng)進(jìn)口醫(yī)療器械。從管理類(lèi)別來(lái)看:包括5項(xiàng)Ⅱ類(lèi)器械產(chǎn)品和11項(xiàng)Ⅲ類(lèi)器械產(chǎn)品。
本網(wǎng)站內(nèi)所有資訊及素材僅供學(xué)習(xí)與科普。如圖片和素材版權(quán)擁有者發(fā)現(xiàn)自己作品被侵權(quán),請(qǐng)及時(shí)向深藍(lán)醫(yī)療提出權(quán)利通知,深藍(lán)醫(yī)療在收到相關(guān)通知后,24小時(shí)內(nèi)移除相關(guān)涉嫌侵權(quán)的內(nèi)容。
上一篇:您真的了解IVD行業(yè)嗎?IVD的眾多術(shù)語(yǔ)可以分得清嗎?
下一篇:行業(yè)資訊 | 國(guó)家藥監(jiān)局新聞發(fā)布會(huì):為高質(zhì)量發(fā)展指明方向



